みなさん、こんにちは。
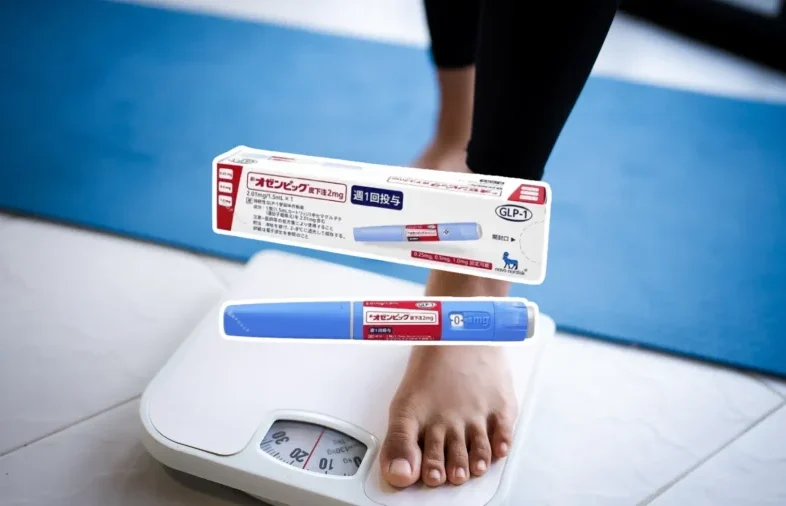
最近、「オゼンピック」や「GLP-1ダイエット」といった言葉を、テレビやSNSで見聞きする機会が増えてきてますよね。
「なんだかすごく痩せるらしい」「でも、副作用が怖い」 そんなイメージをお持ちの方も多いかもしれませんね。
オゼンピック(一般名:セマグルチド)は、もともとは2型糖尿病の治療薬として開発されましたが、その強力な体重減少効果から、世界中で「ダイエット薬」としても大きな注目を集めています。
しかし、その効果が強力であるがゆえに、使い方を誤ると大きなリスクも伴います。
この記事では、オゼンピック(セマグルチド)とは一体どんな薬なのか、その「効果」「副作用」「正しい使い方」、そしてさらに新しい薬として話題の「マンジャロ(チルゼパチド)」と何が違うのかなどについて、臨床研究の具体的なデータに基づきながら、詳しく解説していきます。
オゼンピックとはどんな薬?

まず、オゼンピックがどのようにして効果を発揮するのか、その「仕組み」から見ていきましょう。
オゼンピックの有効成分であるセマグルチドは、「GLP-1(グルカゴン様ペプチド-1)受容体作動薬」というクラスの薬に分類されます 。
GLP-1とは、私たちが食事をして血糖値が上がると、小腸から分泌されるホルモンの一種です。このGLP-1は、体にとって非常に都合の良い働きをすることから、「インクレチン」とも呼ばれています。
オゼンピック(セマグルチド)は、このGLP-1の働きを助け、その効果をより強力に、そして長く持続させるように設計されたお薬なのです。
具体的には、主に以下の3つの働きを通じて、血糖値と体重にアプローチします。
- インスリン分泌の促進 血糖値が高い時だけを選んで、すい臓からのインスリン分泌を強力に後押しします 。血糖値が低い時には作動しにくい、とても賢い仕組みです。
- グルカゴン分泌の抑制 血糖値を上げる作用を持つホルモン「グルカゴン」の分泌を、血糖値に応じて抑え、肝臓で糖が作られるのを抑制します。
- 胃内容排出の遅延と食欲の調節 胃の動きをゆっくりにさせることで、食後の急激な血糖上昇を抑えます 。同時に、脳の視床下部(食欲をコントロールする場所)に直接作用し、満腹感を高め、食欲そのものを抑制します。
この3つの複合的な作用により、オゼンピックは2型糖尿病患者さんの血糖コントロールを劇的に改善するだけでなく、食欲抑制と満腹感の持続によって、強力な「体重減少」という二重の利益をもたらすのが特徴です。
オゼンピックの主な効果①:減量効果

オゼンピック(セマグリチド)でもっとも注目されている効果の1つが「減量効果」ですよね。
オゼンピックは比較少量からでも体重減少効果が認められています。2型糖尿病を発症された3411名を対象とした臨床試験(平均年齢55歳~60歳、平均体重90~98kg、平均BMI32.5~33.6 kg/m2)では、他の治療薬と比較して以下の通り有意に体重を抑えることができました。
- オゼンピック 0.5mg群: -2.35 kg 〜 -4.72 kg
- オゼンピック 1.0mg群: -2.96 kg 〜 -6.76 kg
いずれの試験も30週間~56週間という試験での結果なので、「1カ月ですぐにやせる」というわけではないですが、薬だけの効果としてはかなり大きいものではないでしょうか。
さらに、肥満症の治療薬として同じセマグルチドを成分としながら、用量を調整した「ウゴービ」(セマグルチドが週1回 2.4mg配合されています)では、用量が高い分より強い効果になっておいます。具体的な体重減少効果は以下の通りとなっていますね。(平均体重 105.8 kg, 平均BMI 38.0 kg/m2)
- 平均体重変化(全体):
- セマグルチド 2.4mg群: -14.9%(-15.3 kg)
- プラセボ(偽薬)群: -2.4%(-2.6 kg)
- 体重減少の達成率(臨床的に最も重要):
- 5%以上の減少を達成: 86.4% (vs 31.5%)
- 10%以上の減少を達成: 69.1% (vs 12.0%)
- 15%以上の減少を達成: 50.5% (vs 4.9%)
このように、参加者の半数以上(50.5%)が、68週間で体重の15%以上を減少させたというのはなかなか衝撃的ですね。したがって、ウゴービに関しては、一部の人が糖尿病でなくても処方できる保険治療薬として認められています。
(参照:Once-Weekly Semaglutide Reduces HbA1c and Body Weight in Patients with Type 2 Diabetes Regardless of Background Common OAD: a Subgroup Analysis from SUSTAIN 2–4 and 10)
(参照:Long-Term Efficacy and Safety of Once-Weekly Semaglutide for Weight Loss in Patients Without Diabetes: A Systematic Review and Meta-Analysis of Randomized Controlled Trials)
(参照:Once-Weekly Semaglutide in Adults with Overweight or Obesity)

オゼンピックの主な効果②:2型糖尿病患者の改善効果

もちろんオゼンピック(セマグリチド)は糖尿病の薬ですので、糖尿病の改善効果も認められています。その一番大きな試験は「SUSTAINプログラム」というものです。
SUSTAINプログラムでは、合計3,411人の被験者に対して、オゼンピックが単独で、あるいは他の飲み薬やインスリンと併用して、偽薬(プラセボ)や他の糖尿病治療薬(シタグリプチン、エキセナチドERなど)と比較されています。
主な結果としては以下の通りです。比較対照薬に対する「推定治療差(ETD)」(=オゼンピックによって追加で得られたHbA1c低下幅)は、以下の通りでした。
- オゼンピック 0.5 mg群: HbA1cを -0.32 〜 -0.79 パーセンテージポイント 追加で低下
- オゼンピック 1.0 mg群: HbA1cを -0.38 〜 -1.07 パーセンテージポイント 追加で低下
簡単にいうと、オゼンピックを追加で投薬すると、HbA1cが最大で-1.07%くらいまで下がるというわけですね。
このように、糖尿病の治療薬としても、オゼンピックは非常に優れた効果をしめしています。
オゼンピックの効果③:心臓や血管への良い影響 (SUSTAIN-6試験)
2型糖尿病患者さんの管理において、血糖値を下げることと同じくらい、あるいはそれ以上に重要なのが、最終的なゴールである心筋梗塞や脳卒中といった「心血管疾患」のリスクを減らすことですよね。
これに対してもオゼンピックは、この点でも非常に優れた結果を出しています。
心血管疾患のリスクが高い2型糖尿病患者さん(3,297人)を対象に行われた「SUSTAIN-6」試験では、オゼンピックが心血管イベント(心血管死、非致死的心筋梗塞、非致死的脳卒中)のリスクにどう影響するかが調べられました。
その結果、オゼンピックはプラセボ(偽薬)と比較して、これらの主要心血管イベント(MACE)の発生リスクを、統計学的に有意に26%も低下させたのです。(セマグリチドで群で6.6%、プラセボ群で8.9%の心血管系イベント)
単剤でこれだけ低下させるのは、なかなかない、非常に優れた結果ですね。
この結果をうけて、米国FDA(食品医薬品局)はオゼンピックに対し、「確立されたCVDを有するT2DM成人における主要心血管イベントのリスク低減」という追加の適応を承認しました 。
つまり、オゼンピックは単に血糖値や体重を改善するだけでなく、2型糖尿病患者さんの「生命予後」をも改善しうる、包括的な代謝改善薬であることが示されたのです。
(参照:Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes)
オゼンピックの副作用は?
これほど強力な効果を持つオゼンピックですが、当然ながら副作用(有害事象)もあります。特に知っておくべきは、消化器系の症状です。
最も多いのは「消化器系」の症状

オゼンピックを含むGLP-1受容体作動薬クラスに共通して、最も一般的に報告される有害事象は消化器系の副作用です。(数値はSUSTAIN-1での試験での数値)
- 吐き気(悪心)・嘔吐:20~24%(vs プラセボ 8%)
- 下痢:11~13%(vs. プラセボ2%)
5人に1人は吐き気がでやすいというのは、なかなか副作用の頻度としては多いと思います。実際、高用量(2.4mg)を使用したSTEP 1試験では、消化器症状が理由で治療を中止した人の割合は、セマグルチド群で4.5%(プラセボ群は0.8%)いました。20人に1人は副作用が辛くてやめてしまうのですね。
ただし、消化器症状の多く(98%)は、軽度から中等度であり、継続できるとされています。また、副作用は、治療の開始時や用量の増加時には強いものの、治療を継続していくうちに体が薬剤に慣れ、軽快していく傾向があることがわかっています。
ですので、「吐き気が出たからやめてしまおう」と思わずに続けることで、徐々に体が慣れてきます。ある意味これはセマグリチドのもつ「胃の内容排泄遅延によって食べられなくする効果」そのものともいえるので、「多少の胃もたれは出るものなのだな」と思っていただけるといいですね。(もちろん、過度な無理は禁物です)
その他の重篤なリスクは?
消化器症状の他にも、以下の報告がありますが、いずれも軽度であり、忍容性は比較的高い薬剤です。
- 胆石症 (Cholelithiasis) :GLP-1受容体作動薬のクラス全体で、胆石症の発生率がプラセボ群より高いことが示されています(STEP 2.4mg群で1~3%未満)。ただしこれは、薬剤の直接的な毒性というよりも、オゼンピックがもたらす「急速かつ大幅な体重減少」に伴う二次的な生理的変化(胆汁の組成変化など)が原因である可能性が最も高いと考えられています。
- 急性腎障害 (Acute Kidney Injury, AKI) :AKIの症例報告はありますが、その多くは、重度の嘔吐や下痢による「脱水(体液量減少)」が引き金となっていました。オゼンピックが直接的に腎臓に毒性を持つというよりは、重度の消化器症状の管理が不十分だった場合の二次的な合併症である可能性が高いと指摘されています。
- 膵炎 (Pancreatitis) :GLP-1受容体作動薬の導入初期から懸念されていましたが、大規模臨床試験のデータでは、急性膵炎の発生率は0~1%未満と非常に稀でした。
オゼンピックによるがんのリスクは?(膵臓がん・甲状腺がん)

安全性に関する最も重大な懸念の一つに、がん(特に膵臓がんと甲状腺がん)のリスクがありました。
この点について、2023年に発表された、臨床試験(RCT)とリアルワールドデータを統合した大規模なメタアナリシス(複数の研究を統計的に解析した、非常に信頼性の高い研究)では、膵臓がんと甲状腺がんについて以下のように結論づけています。
- 膵臓がん: セマグルチドの使用は、他の血糖降下薬と比較して、膵臓がんのリスク増加と関連していませんでした(オッズ比 0.40; 統計的有意差なし)。
- 甲状腺がん: 甲状腺がんについても、他の血糖降下薬との間に統計的に有意なリスク差は検出されませんでした(オッズ比 1.19; 統計的有意差なし)。
本論文の著者らも、「セマグルチドの使用は、いかなるタイプのがんのリスク増加とも関連していない」と結論付けていますね。
したがって、「オゼンピックによってがんになりやすい」とはあまり考えなくてもよいのではないでしょうか。
(参照:Semaglutide and cancer: A systematic review and meta-analysis)
オゼンピックの正しい「使い方」
ここでは、一番よく処方される「オゼンピック®皮下注2mg」の具体的な使い方を説明していきます。
ステップ1:注射の準備と注射針の取りつけ
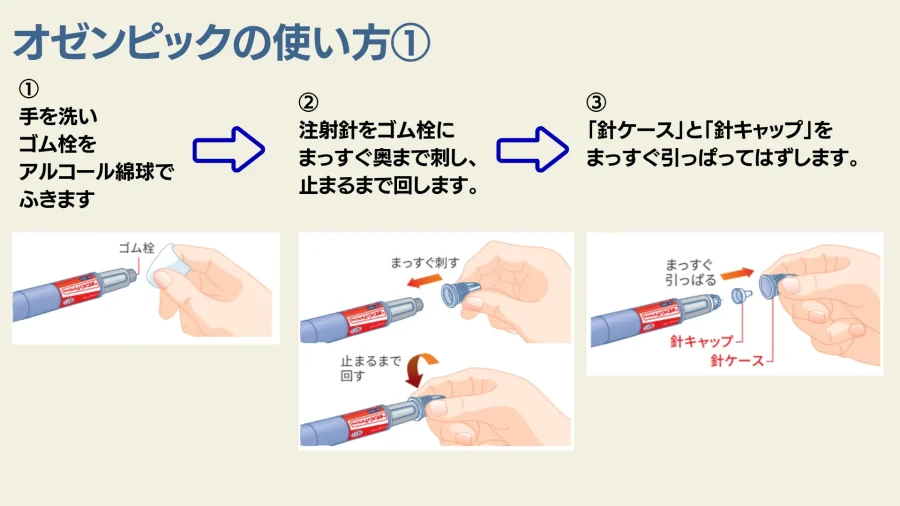
- 手を洗う: まず、手指を石けんでよく洗います。
- ペンの準備: オゼンピック®のキャップをはずし、先端のゴム栓をアルコール綿で拭きます。
- 注射針の準備: 新しい注射針の保護シールをはがします。
- 針の取りつけ: 注射針をペンのゴム栓にまっすぐ奥まで刺し、止まるまで回して取り付けます。
- キャップをはずす: 「針ケース」(外側のキャップ)と「針キャップ」(内側のキャップ)を、両方ともまっすぐ引っぱってはずします。
- 注意: はずした「針ケース」は、注射後に針をはずす際に使用するため、捨てずに取っておいてください(針キャップは捨てます)。
ステップ2:動作確認(※初回使用時のみ)
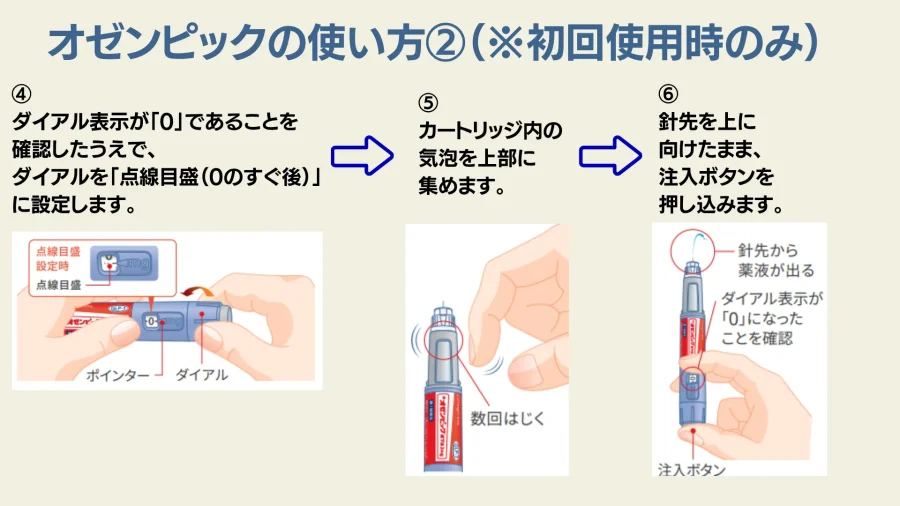
新しいペンを初めて使う時のみ、薬液が正しく出るかを確認(動作確認)します 。 2回目以降の使用時は、この動作確認は不要です。
- ダイアル設定: ダイアル表示が「0」であることを確認し、ダイアルを回して「点線目盛(0のすぐ後)」に設定します。
- 気泡を集める: 針先を上に向けたまま、カートリッジ(薬液が入っている部分)を指で軽く数回はじき、気泡を上部に集めます。
- 薬液の確認: 針先を上に向けたまま、注入ボタンを押し込みます 。ダイアル表示が「0」になったことを確認し、針先から薬液が出ることを確認します。
- 薬液が出ない場合は、新しい注射針に交換し、再度この動作確認を行ってください。
ステップ3:投与量(注射する量)の設定

- 「0」の確認: ダイアル表示が「0」になっていることを確認します。
- ダイアルを回す: 注入ボタンに指が触れないように注意しながら 、ダイアルを回し、主治医から指示された量(0.25mg、0.5mg、1.0mgのいずれか)を「ポインター」に正確に合わせます。
- 注意: 0.25mg、0.5mg、1.0mg以外のところに設定して投与しないでください。
ステップ4:注射の実施
- 注射場所の決定: 注射する場所は、「おなか(腹壁)」「上腕部の外側」「太もも(大腿部)の外側」が適しています。
- 場所のローテーション: 毎回同じ部位(例:「おなか」なら「おなか」)に注射しますが、皮膚が硬くなるのを防ぐため、前回注射した場所から少なくとも2〜3cm(指2本以上)ずらして注射してください。
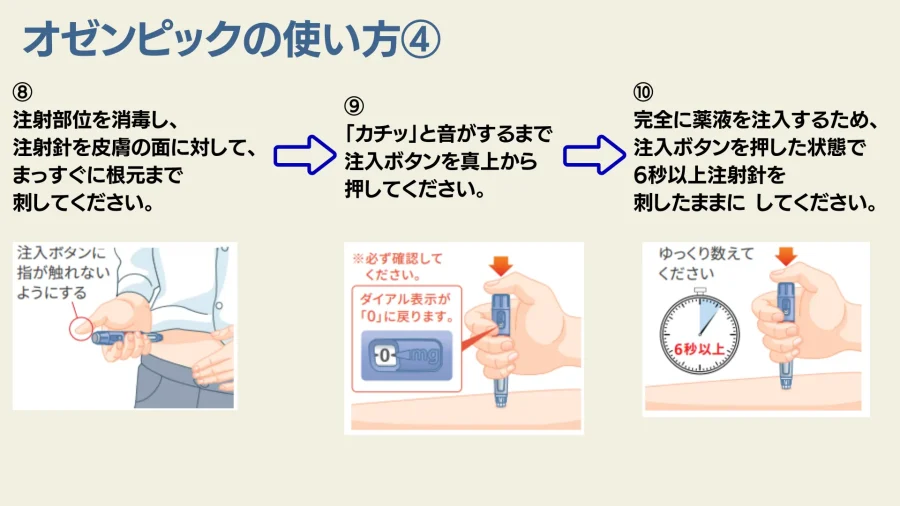
- 消毒と注射: 注射部位を消毒し、注射針を皮膚の面に対してまっすぐに根元まで刺してください。
- 薬液の注入: 「カチッ」と音がするまで、注入ボタンを真上から押してください。ダイアル表示が「0」に戻るのを確認します。
- 【重要】6秒間待つ: 完全に薬液を注入するため、注入ボタンを押した状態で、6秒以上そのまま(注射針を刺したまま)待ってください。
- 針を抜く: 6秒以上数えたら、注入ボタンを押したまま注射針を皮膚から抜きます。
ステップ5:注射針のはずし方と廃棄
- 【重要】すぐに針をはずす: 注射が終わったら、必ず直ちに注射針をはずしてください 。
- 針ケースをかぶせる: ステップ1で取っておいた「針ケース」を、針にまっすぐかぶせます 。
- 注意: 針刺し事故を防ぐため、はずした「針キャップ」(内側のキャップ)は絶対につけないでください 。
- 針をはずす: 針ケースごと回して、まっすぐ引っぱって注射針をはずします 。
- 廃棄: はずした注射針は、感染症を防ぐため、医療従事者の指示に従って正しく廃棄してください 。
- ペンの保管: 注射針をはずした後、ペンのキャップをつけて保管します 。
(参照:novo nordisk「オゼンピック皮下注2mgによる2型糖尿病治療ガイド」)
【注意】使う際には少ない量から始めてください

ここで、必ず守ってほしいことがあります。それはオゼンピックを始める際には、必ず少ない量から始めてほしいということです。
というのも、オゼンピックは消化器症状を中心とした副作用が出やすいのがデメリットです。実際、途中で離脱してしまう人もいます。しかし、少ない量から始めることで、安全に副作用も少なく続けやすくなっています。
具体的には次の通りです。
- 導入期(Week 1-4):
- 0.25 mg を週1回、4週間投与。(注:この用量は治療用量ではなく、体を薬剤に順応させるための「導入用量」です )
- ステップ1(Week 5-8):
- 0.5 mg を週1回に増量し、最低4週間投与。
- ステップ2(Week 9以降):
- さらに追加の血糖コントロールが必要な場合、1.0 mg を週1回に増量し、最低4週間投与。
- ステップ3(Week 13以降): * さらに追加が必要な場合、2.0 mg を週1回に増量できる(T2DM治療における最大用量 )。
なぜ、各ステップで「最低4週間」という期間が定められているのでしょうか? それは、オゼンピックの「薬物動態(Pharmacokinetics, PK)」に理由があります。
オゼンピック(セマグルチド)は、体からの消失半減期(血中濃度が半分になるまでの時間)が**約1週間(~165時間)と非常に長い薬剤です。
そのため、週1回の投与を開始した後、血中濃度が安定した状態(定常状態)に達するまでに、4~5週間を要するのです。
つまり、「最低4週間」という期間は、ある用量レベルでの安定した血中濃度に、患者さんの消化器系が完全に順応するための、医学的に必須な時間なのです。
このステップを省略したり、自己判断で性急に増量したりすることは、重度の消化器症状を誘発し、結果として治療そのものを続けられなくなる(脱落)リスクに直結します。
ついつい「早く減量したい!」と思うあまり、投与量を多くはじめてしまう人がいますが、絶対にやめましょう。

オゼンピックとマンジャロの違いは?
オゼンピック(セマグルチド)が治療に革命をもたらした一方で、近年、それをさらに凌駕する可能性のある薬剤として「マンジャロ(一般名:チルゼパチド)」が登場し、大きな注目を集めています。
両者は何が違い、どちらがより優れているのでしょうか?
① オゼンピックとマンジャロは作用メカニズムが違う
そもそもオゼンピックとマンジャロでは、作用するポイントが違います。
- オゼンピック(セマグルチド):
- 単一アゴニスト:GLP-1受容体にのみ選択的に作用します。
- マンジャロ(チルゼパチド):
- デュアルアゴニスト(ツインクレチン):GLP-1受容体に加え、もう一つの主要なインクレチンホルモンであるGIP(グルコース依存性インスリン分泌刺激ポリペプチド)の受容体にも同時に作用します 62。
簡単にいうと、マンジャロは本来のオゼンピックが作用する「GLP-1」に加えて、「GLP-1」に相乗効果がある「GIP」にも作用する薬ですね。この「GIP作用の追加」こそが、両薬剤の臨床効果の差を生み出す最大の要因と考えられています。
② オゼンピックとマンジャロ、直接対決の結果は? (SURPASS-2試験)
では、オゼンピックとマンジャロ、効果の違いはどれくらいあるのでしょうか。
「SURPASS-2」試験では、2型糖尿病患者さん、1879人を対象に、マンジャロ(5mg, 10mg, 15mgの3用量)とオゼンピック(1mg)の有効性・安全性を40週間にわたり「直接比較試験」をしています。
その結果は、明確でした。
【血糖コントロール(HbA1c)の比較】
マンジャロは、全3用量すべてにおいて、オゼンピック1mgに対し「優越性(Superiority)= 勝ち」を達成しました。ベースラインからの平均HbA1c低下量は以下の通りです。
- オゼンピック 1.0 mg群: -1.86 %
- マンジャロ 5 mg群: -2.01 %
- マンジャロ 10 mg群: -2.24 %
- マンジャロ 15 mg群: -2.30 %
【体重減少の比較】
体重減少においても、マンジャロはオゼンピック1mgに対し、用量依存的な「優越性(勝ち)」を示しました。オゼンピック1.0mg群に対して「追加で」体重減少が認められた量は以下の通りです。
- マンジャロ 5 mg群: -1.9 kg
- マンジャロ 10 mg群: -3.6 kg
- マンジャロ 15 mg群: –5.5 kg
この試験結果で最も衝撃的だったのは、マンジャロの最低用量(5mg)でさえ、オゼンピックの(当時の)最高用量(1mg)に対し、血糖コントロールと体重減少の両方で統計的に有意に勝利したことですね。
➂ 副作用(忍容性)の違いは?
では、これほど効果が強いマンジャロは、副作用も比例して強いのでしょうか?
SURPASS-2試験によると、主な消化器系有害事象の発生率は、高用量どうしで比較すると、若干マンジャロの方が副作用が出やすくなっていますね。
| 有害事象 (%) | オゼンピック 1.0 mg群 | マンジャロ 5 mg群 | マンジャロ 10 mg群 | マンジャロ 15 mg群 |
| 吐き気 | 18 % | 17 % | 22 % | 22 % |
| 下痢 | 12 % | 16 % | 13 % | 14 % |
| 嘔吐 | 8 % | 6 % | 8 % | 10 % |
しかし、マンジャロ(特に10mg, 15mg)が、オゼンピック1mgよりも「追加で-5.5kg」といった劇的な有効性を示したにもかかわらず、消化器症状の発生率が意外と悪化しておらず、数%増加にとどまっているのはかなり衝撃的です。
これは、GIPへのデュアルアゴニズムが、GLP-1による消化器症状を何らかのメカニズムで緩和している可能性もいわれています。
したがって、総括すると(仮に自費で体重減少を目的でする場合)「体重減少だけ考えるなら『マンジャロ』に軍配が上がるが、逆にマンジャロをやめる時のリバウンドが心配な場合や副作用が心配という人、少量から始めたいという方は『オゼンピック』を選ぶ」と考えるとよいでしょう。
(参照:Tirzepatide versus Semaglutide Once Weekly in Patients with Type 2 Diabetes)
(参照:Tirzepatide as Compared with Semaglutide for the Treatment of Obesity)
話題の「オゼンピック顔(Ozempic Face)」とは?

最後に、セマグルチド(オゼンピックやウゴービ)の使用が世界的に急増するにつれ、美容医療の分野で「オゼンピック顔(Ozempic Face)」と呼ばれる現象があつめていますよね。これは何かについて説明します。
①「オゼンピック顔」は医学的用語ではありません
まず、「オゼンピック顔」は正式な医学的診断名ではありません。GLP-1受容体作動薬の使用に関連して生じる、「顔がこける」ような特徴的な顔面の美容的変化を指す一般用語(メディア用語)です 。
そして最も重要なことは、この現象は、薬剤が顔に直接作用する「副作用」ではない、という点です。
そうではなく、オゼンピックやマンジャロは急激に体重減少が期待できる薬です。人間、運動をせず筋肉もつけないまま体重が大幅に減少すると、二次的に顔も変わってしまうという意味になります。
② なぜオゼンピックで「顔がこける」のか?
ではなぜオゼンピック顔といわれるように、「顔がこける」ようになってしまうのか。考えられている原因については次の通りとなっています。
- オゼンピックは全身の脂肪組織を強力に減少させますよね。この作用は、当然ながら顔面の皮下脂肪にも例外なく及びます。
- もともと顔面の脂肪は、皮膚を深層で支える「足場」として機能しています。この支持組織が急速に失われると、顔は「くぼみ」や「こけ」た外観になっています、
- 同時に、皮膚(特に加齢で弾力性が低下した皮膚)は、急速なボリューム減少に間に合うように収縮していきません。
- その結果、脂肪という「支え」を失った皮膚が余り、「たるみ」やシワとして顕在化してオゼンピック顔と呼ばれるような顔つきになるのです。
しかし、上記の現象は、オゼンピックに特有のものではありません。例えば、肥満外科手術などで同程度(-15%以上)の急速な体重減少を達成した場合でも、顔面には全く同じ変化(脂肪の萎縮と皮膚の弛緩)が生じることが知られていますね。
したがって、「オゼンピック顔」は、薬剤の副作用ではなく、あまりに急激にやせすぎた結果によるものと解釈した方が自然です。
当院でもオゼンピックを自費でも取り扱っています

「自力でなかなかダイエットできない…」「マンジャロよりも副作用が少ない薬から始めたい」という方のために、オゼンピックの自費処方を当院でも始めました。(もちろん高度糖尿病の方など、適切な方には保険診療でもオゼンピックを処方しています)
オゼンピックの値段は以下の通りです。(診療代込み)
| オゼンピック 2mg | 20,000円 |
例えば、オゼンピックは0.25mgが開始用量なので、0.25mgから始める場合、およそ2カ月くらいもつことになります。0.25mg4週間おこなったのち、0.5mgに増量する場合は約1.5カ月の分量ですね。
0.5mgの場合は1カ月分の値段となります。
また、当院では、内服薬のダイエット治療薬「リベルサス」「マンジャロ」も自費投薬しています。しかし、大切なことは前述した通り、「きちんと安全性を考えながらモニタリングされていること」だと思います。
そこで当院では適切な時期に採血をうながし、モニタリングするようにしています(自費採血:3,000円)。もちろん、過度にやせている方などは、「得られる利益」よりも「体の負担」の方が大きくなる可能性があるので、対象とはなり得ません。自費でも処方する以上、処方する側の責任もあると思っているからです。
「どうしても自分の力ではダイエットできない」という方は、ぜひ当院にご相談ください。体全体のことを考えた上で、適切にアドバイスさせていただきます。
【この記事を書いた人】
一之江駅前ひまわり医院院長の伊藤大介と申します。プロフィールはこちらを参照してください。
あわせてこちらもオススメです
- マンジャロのダイエット効果と副作用について【値段も掲載】
- リベルサスのダイエット効果や副作用・飲み方について
- ダイエットに漢方は効果がある?減量に使う漢方の種類と特徴について論文から解説
- 寿命を延ばす食べ物は?長寿の秘訣を医学論文から検証します!
- 地中海食は認知症やダイエットに効果がある?地中海食の論文によるエビデンスを紹介!
- 胃腸の調子が悪い時の食事について【おすすめな食べ物・避けるべき食べ物】
- 脂肪肝におすすめの食事改善法について解説【減量・コーヒー・アルコール】
- 脂肪肝の症状や原因・薬物治療についてわかりやすく解説
















この記事へのコメントはありません。